人民網北京10月17日電 (曾璇)為加強醫療器械質量監督管理,保障醫療器械產品使用安全有效,國家食品藥品監督管理總局組織對紅外輻射治療設備、C反應蛋白檢測試劑2個品種79批(台)的產品進行了質量監督抽檢。其中,5家醫療器械生產企業的1個品種8台醫療器械產品被抽檢項目不符合標准規定。
具體不合格產品情況如下:
紅外輻射治療設備5家企業8台產品。四川恆明科技開發有限公司生產的2台特定電磁波譜治療器,加熱器表面溫度不均勻度不符合標准規定﹔重慶長樂硅酸鹽有限責任公司生產的1台特定電磁波譜治療器、重慶華倫醫療器械有限公司生產的2台特定電磁波(TDP)治療器,加熱器表面溫度誤差、加熱器表面溫度不均勻度不符合標准規定﹔哈爾濱億爾諾醫學科技有限公司生產的1台紅外光治療儀,指示燈和按鈕不符合標准規定﹔重慶鑫億醫療器械有限公司生產的2台TDP特定電磁波治療器,傾倒防護不符合標准規定。
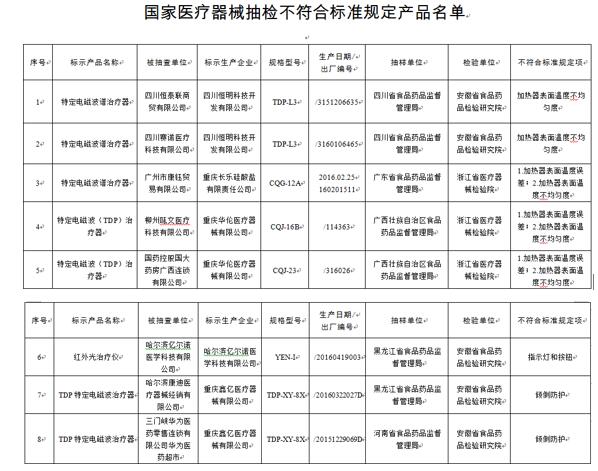
(圖片來源:國家食品藥品監督管理總局官網)
此外,被抽檢項目為標識標簽、說明書等項目不符合標准規定的醫療器械產品,涉及4家醫療器械生產企業的1個品種4台,具體為:
紅外輻射治療設備4家企業4台產品。重慶長樂硅酸鹽有限責任公司生產的1台特定電磁波譜治療器,設備或設備部件的外部標記不符合標准規定﹔深圳市康益生物科技有限公司生產的1台磁紅外加壓創面氧合儀、哈爾濱億爾諾醫學科技有限公司生產的1台紅外光治療儀,使用說明書不符合標准規定﹔江蘇杰益美醫療器械有限公司生產的1台遠紅外線溫熱治療器,外部標記、使用說明書、設備或設備部件的外部標記不符合標准規定。